“百万肿瘤神药”CAR-T疗法到底是如何“清零”癌细胞的?
2023-01-20
6739
2021下半年以来,有“百万肿瘤神药”之称的CAR-T疗法接连斩获多个热搜,这一昂贵而特别的新疗法逐渐走入大众视野,但大多数人都是知其然而不知其所以然, 今天小编就给大家盘一盘,CAR-T到底是如何“清零”癌细胞的。
今天小编就给大家盘一盘,CAR-T到底是如何“清零”癌细胞的。
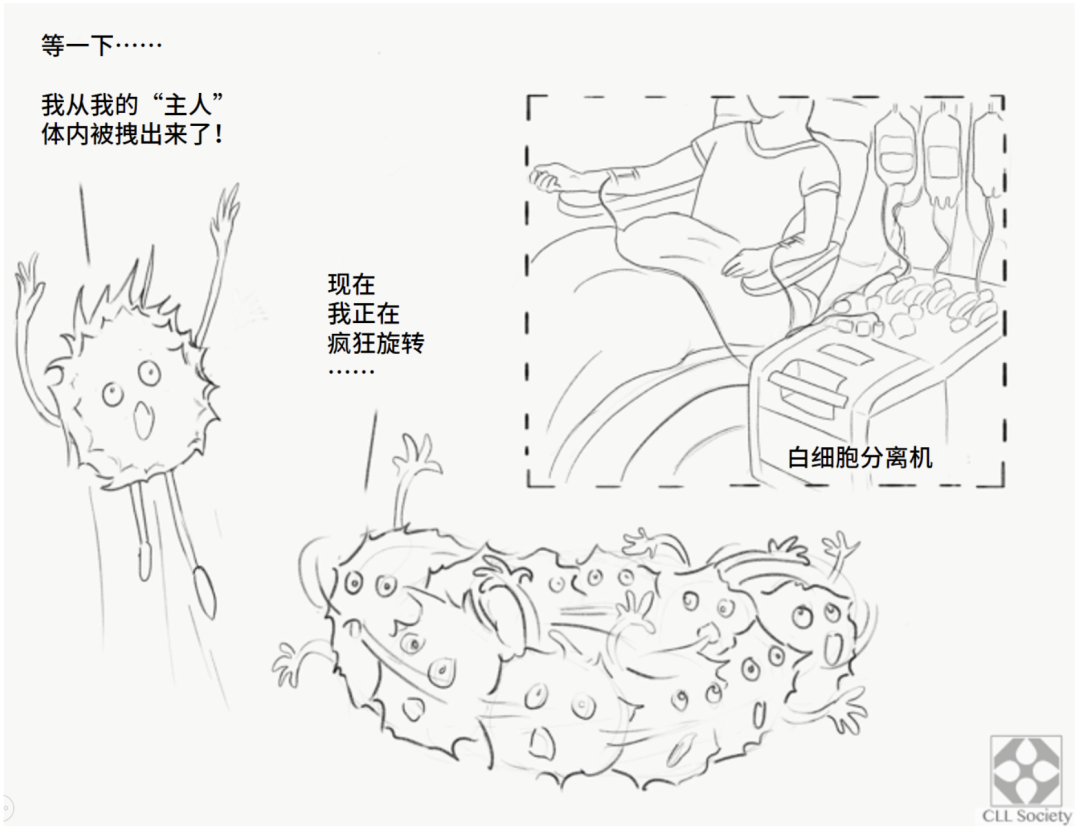
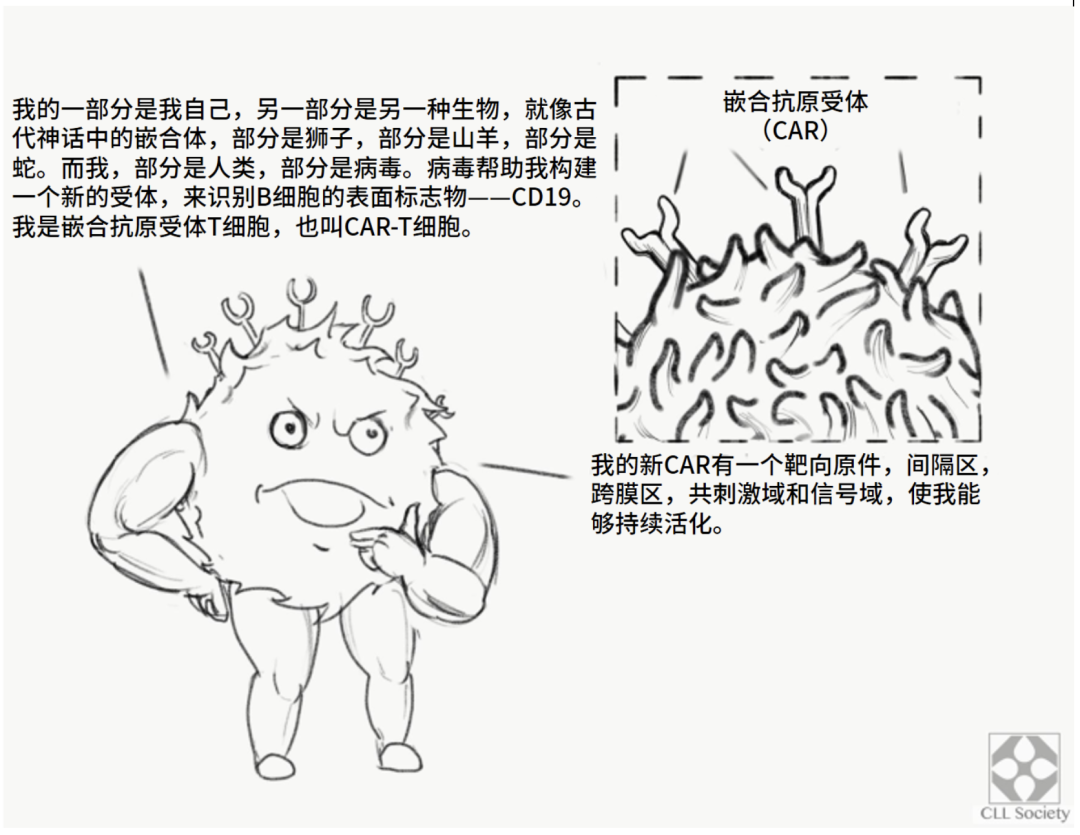
CAR-T即嵌合抗原受体T细胞(CAR-T)疗法,是细胞疗法的一种,先由医疗机构采集患者的外周血淋巴细胞,再送往药企或实验室通过基因修饰技术将T细胞改造为CAR-T,改造后的CAR-T细胞可以识别并杀死相应的肿瘤细胞,最后经过扩增生产后将这些CAR-T细胞通过静脉输液的方式重新输回患者体内。大家都有疑问,患者本身的T细胞杀不死肿瘤细胞,CAR-T到底发生了哪些变化,怎么就能杀死肿瘤细胞了呢?小编找到了一幅漫画来帮助大家理解。

(如有版权问题,请联系我们删除)
目前,国内已有2款CAR-T细胞产品上市,适应症包括复发难治性大B细胞淋巴瘤和滤泡性淋巴瘤。那么,患者的治疗流程是怎样的呢?首先,医生要对患者进行全面评估从而判断患者是不是适合进行CAR-T治疗,符合治疗条件的患者则按照流程进行白细胞单采,之后半个月左右是CAR-T细胞生产期,在此期间医生根据患者自身及其疾病情况判断是否需要其他治疗,在CAR-T细胞生产完成并运送至治疗中心后,患者即可回输CAR-T细胞,回输前需要进行细胞清除性化疗,回输后需要进行密切的随访监测。
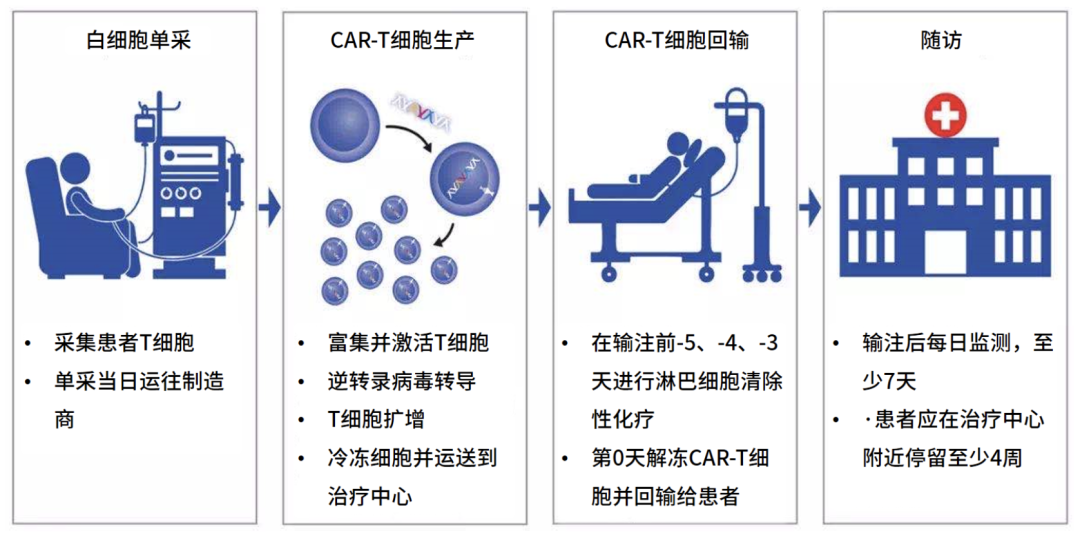
图片来源:JAMA Oncol. doi:10.1001/jamaoncol.2019.3869.
以上我们说的都是自体细胞来源的CAR-T,自体CAR-T的制备工艺非常复杂,很多步骤都需要人工操作,耗时耗力,难以扩大。复杂的工艺以及针对患者的个性化定制导致成本高昂,使患者的可及性大大降低(如:复星凯特的阿基仑赛注射液定价120万元/支,药明巨诺的瑞基奥仑赛注射液129万元/支)。而通用型CAR-T带来了破局之道。通用型CAR-T又称异体CAR-T,它是使用来自健康志愿者的T细胞来生产CAR-T细胞。它能够通过工业化生产和规模化制造工艺,来降低生产成本,并且可以生产成批冷冻保存的CAR-T细胞,使患者立即获得治疗,因此又称为"现货型"CAR-T。但是目前全球还没有通用型CAR-T获批上市,均处在临床研究阶段,仅参与临床试验的患者可及。在21世纪的今天,CAR-T技术日新月异,已经出现了第5代产品,除了技术的升级,治疗靶点和疾病适应症也有所拓展。除了靶向B细胞淋巴瘤的CD19、多发性骨髓瘤的BCMA、急性髓系白血病的CD33、胃肠道肿瘤的Claudin18.2(CLDN18.2)、肝癌的GPC3等靶点的CAR-T细胞研发外,双靶点CAR-T甚至三靶点CAR-T的研发也正如火如荼,目前均处于临床前或临床研究阶段,患者只能通过参与临床试验的途径接受相应的CAR-T治疗。- 有可测量病灶(病灶大于1cm),且肝部最大病灶不超过3cm,不多于5个,其他部位病灶不超过7cm
年龄:18-75岁
- 经病理组织学或者细胞学检查确诊的晚期肝细胞癌(HCC)患者,按照巴塞罗那肝癌分级标准(BCLC)分期为 C 期或不适于接受局部治疗/局 部治疗进展的 B 期(局部治疗包括消融治疗、介入和放射治疗)。
- 对肿瘤组织样品的免疫组化法检测为 GPC3 阳性(定义为由病理标本 IHC 中 GPC3 阳性细胞比例≥25%且染色度≥1+);
- 若患者 HBsAg 阳性或 HBcAb 阳性,需满足 HBV-DNA<2000 IU/ml。 HBsAg 阳性患者必须接受抗病毒治疗
年龄:14~60 岁
- CR 后12个月内复发者;或在12个月后复发但经过常规化疗无效者;
年龄:18-75岁(包含临界值)
经组织学证实的B细胞淋巴瘤,淋巴瘤细胞表达CD19/CD20/CD22至少一个;
至少有一个可评估的肿瘤灶:结内病灶最长径>1.5cm,结外病灶最长径>1.0cm;
足够的造血、肝、肾器官功能储备
年龄≥18岁
有可测量病灶:血清单克隆副蛋白(M-蛋白)水平≥1.0 g/dL 或尿 M 蛋白水平≥200 mg/24 小时;或血清或尿液中无可测量病灶的轻链型多发性骨髓瘤:血清免疫球蛋白 游离轻链≥10 mg/dL 且免疫球蛋白κ/λ游离轻链比异常;
接受过一种 PI 和一种 IMiD(除外沙利度胺)治疗;
既往接受过至少 3 线多发性骨髓瘤治疗,每线治疗至少有 1 个完整治疗周期,除非对治疗方案的最佳缓解状况记录为疾病进展;或既往对任一种 PI 和任一种 IMiD 难治或不耐受的受试者
足够的造血、肝、肾器官功能储备
流式检测外周血或骨髓的白血病细胞表达 CD19/CD20/CD22 中至少一个;
病理学确认的复发/难治 ALL,必须满足下列条件之一:
CR 后 12 个月内复发,或 12 个月后复发但再次诱导治疗无效的患者;
2 次或 2 次以上的骨髓复发;
费城染色体阳性(Ph+)的 ALL 患者无法耐受 TKI 治疗,或 2 线以上 TKI 治疗失败的患者,或者存在 TKI 治疗禁忌症的患者;
 今天小编就给大家盘一盘,CAR-T到底是如何“清零”癌细胞的。
今天小编就给大家盘一盘,CAR-T到底是如何“清零”癌细胞的。